TEMPERATURA
TEMPERATURA
Los átomos y moléculas en una sustancia no siempre se mueven a la misma velocidad. Esto significa que hay un rango de energía (energía de movimiento) en las moléculas. En un gas, por ejemplo, las moléculas se mueven en direcciones aleatorias y a diferentes velocidades - algunas se mueven rápido y otras más lentamente.
| La temperatura es una medida del calor o energía térmica de las partículas en una sustancia. Como lo que medimos en sus movimiento medio, la temperatura no depende del número de partículas en un objeto y por lo tanto no depende de su tamaño. Por ejemplo, la temperatura de un cazo de agua hirviendo es la misma que la temperatura de una olla de agua hirviendo, apesar de que la olla sea mucho más grande y tenga millones y millones de moléculas de agua más que el cazo. |
Nosotros experimentamos la temperatura todos los días. Cuando hace calor o cuando tenemos fiebre sentimos calor y cuando está nevando sentimos frío. Cuando estamos hirviendo agua, hacemos que la temperatura aumente y cuando estamos haciendo polos o paletas de helado esperamos que la temperatura baje.
La temperatura de un gas ideal monoatómico es una medida relacionada con la energía cinética promedio de sus moléculas al moverse. En esta animación, la relación del tamaño de los átomos de helio respecto a su separación se conseguiría bajo una presión de 1950 atmósferas. Estos átomos a temperatura ambiente tienen una cierta velocidad media (aquí reducida dos billones de veces).
La temperatura es una magnitud referida a las nociones comunes de caliente o frío. Por lo general, un objeto más "caliente" tendrá una temperatura mayor, y si fuere frío tendrá una temperatura menor. Físicamente es una magnitud escalar relacionada con la energía interna de un sistema termodinámico, definida por el principio cero de la termodinámica. Más específicamente, está relacionada directamente con la parte de la energía interna conocida como "energía sensible", que es la energía asociada a los movimientos de las partículas del sistema, sea en un sentido traslacional, rotacional, o en forma de vibraciones. A medida que es mayor la energía sensible de un sistema, se observa que está más "caliente"; es decir, que su temperatura es mayor.
En el caso de un sólido, los movimientos en cuestión resultan ser las vibraciones de las partículas en sus sitios dentro del sólido. En el caso de un gas ideal monoatómico se trata de los movimientos traslacionales de sus partículas (para los gases multiatómicos los movimientos rotacional y vibracional deben tomarse en cuenta también).
Dicho lo anterior, se puede definir la temperatura como la cuantificación de la actividad molecular de la materia.
Multitud de propiedades fisicoquímicas de los materiales o las sustancias varían en función de la temperatura a la que se encuentren, como por ejemplo su estado (sólido, líquido, gaseoso, plasma), su volumen, la solubilidad, la presión de vapor, su color o la conductividad eléctrica. Así mismo es uno de los factores que influyen en la velocidad a la que tienen lugar las reacciones químicas.
La temperatura es una propiedad física que se refiere a las nociones comunes de calor o ausencia de calor, sin embargo su significado formal en termodinámica es más complejo, a menudo el calor o el frío percibido por las personas tiene más que ver con la sensación térmica (ver más abajo), que con la temperatura real. Fundamentalmente, la temperatura es una propiedad que poseen los sistemas físicos a nivel macroscópico, la cual tiene una causa a nivel microscópico, que es la energía promedio por partícula.
La temperatura está íntimamente relacionada con la energía interna y con la entalpía de un sistema: a mayor temperatura mayores serán la energía interna y la entalpía del sistema.
La temperatura es una propiedad intensiva, es decir que no depende del tamaño del sistema, sino que es una propiedad que le es inherente y no depende ni de la cantidad de sustancia ni del material del que este compuesto.
Ley cero de la termodinámica
Un termómetro debe alcanzar el equilibrio térmico antes de que su medición sea correcta.
Antes de dar una definición formal de temperatura, es necesario entender el concepto de equilibrio térmico. Si dos partes de un sistema entran en contacto térmico es probable que ocurran cambios en las propiedades de ambas. Estos cambios se deben a la transferencia de calor entre las partes. Para que un sistema esté en equilibrio térmico debe llegar al punto en que ya no hay intercambio neto de calor entre sus partes, además ninguna de las propiedades que dependen de la temperatura debe variar.
Una definición de temperatura se puede obtener de la Ley cero de la termodinámica, que establece que si dos sistemas A y B están en equilibrio térmico, con un tercer sistema C, entonces los sistemas A y B estarán en equilibrio térmico entre sí. Este es un hecho empírico más que un resultado teórico. Ya que tanto los sistemas A, B, y C están todos en equilibrio térmico, es razonable decir que comparten un valor común de alguna propiedad física. Llamamos a esta propiedad temperatura.
.
Segunda ley de la termodinámica
También es posible definir la temperatura en términos de la segunda ley de la termodinámica, la cual dice que la entropía de todos los sistemas, o bien permanece igual o bien aumenta con el tiempo, esto se aplica al Universo entero como sistema termodinámico. La entropía es una medida del desorden que hay en un sistema. Este concepto puede ser entendido en términos estadísticos, considere una serie de tiros de monedas. Un sistema perfectamente ordenado para la serie, sería aquel en que solo cae cara o solo cae cruz. Sin embargo, existen múltiples combinaciones por las cuales el resultado es un desorden en el sistema, es decir que haya una fracción de caras y otra de cruces. Un sistema desordenado podría ser aquel en el que hay 90% de caras y 10% de cruces, o 60% de caras y 40% de cruces. Sin embargo es claro que a medida que se hacen más tiros, el número de combinaciones posibles por las cuales el sistema se desordena es mayor; en otras palabras el sistema evoluciona naturalmente hacia un estado de desorden máximo es decir 50% caras 50% cruces de tal manera que cualquier variación fuera de ese estado es altamente improbable.
Hay que notar que para Tf = 0 K la eficiencia se hace del 100%, temperaturas inferiores producen una eficiencia aún mayor que 100%. Ya que la primera ley de la termodinámica prohíbe que la eficiencia sea mayor que el 100%, esto implica que la mínima temperatura que se puede obtener en un sistema microscópico es de 0 K. Reordenando la ecuación (4) se obtiene:
Unidades de temperatura
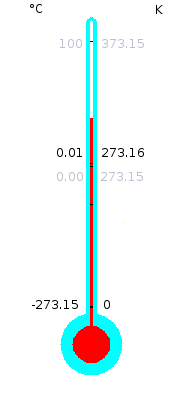
Se comparan las escalas Celsius y Kelvin mostrando los puntos de referencia anteriores a 1954 y los posteriores para mostrar cómo ambas convenciones coinciden. De color negro aparecen el punto triple del agua (0,01 °C, 273,16 K) y el cero absoluto (-273,15 °C, 0 K). De color gris los puntos de congelamiento (0,00 °C, 273,15 K) y ebullición del agua (100 °C, 373,15 K).
Las escalas de medición de la temperatura se dividen fundamentalmente en dos tipos, las relativas y las absolutas. Los valores que puede adoptar la temperatura en cualquier escala de medición, no tienen un nivel máximo, sino un nivel mínimo: el cero absoluto.[1] Mientras que las escalas absolutas se basan en el cero absoluto, las relativas tienen otras formas de definirse.
Relativas
- Grado Celsius (°C). Para establecer una base de medida de la temperatura Anders Celsius utilizó (en 1742) los puntos de fusión y ebullición del agua. Se considera que una mezcla de hielo y agua que se encuentra en equilibrio con aire saturado a 1 atm está en el punto de fusión. Una mezcla de agua y vapor de agua (sin aire) en equilibrio a 1 atm de presión se considera que está en el punto de ebullición. Celsius dividió el intervalo de temperatura que existe entre éstos dos puntos en 100 partes iguales a las que llamó grados centígrados °C. Sin embargo, en 1948 fueron renombrados grados Celsius en su honor; así mismo se comenzó a utilizar la letra mayúscula para denominarlos.
Las escalas que asignan los valores de la temperatura en dos puntos diferentes se conocen como escalas a dos puntos. Sin embargo en el estudio de la termodinámica es necesario tener una escala de medición que no dependa de las propiedades de las sustancias. Las escalas de éste tipo se conocen como escalas absolutas o escalas de temperatura termodinámicas.
Sistema Internacional de Unidades (SI)
- Kelvin (K) El Kelvin es la unidad de medida del SI. La escala Kelvin absoluta es parte del cero absoluto y define la magnitud de sus unidades, de tal forma que el punto triple del agua es exactamente a 273,16 K.[1]
Aclaración: No se le antepone la palabra grado ni el símbolo º.
Sistema Anglosajón de Unidades:
- Grado Rankine (°R o °Ra). Escala con intervalos de grado equivalentes a la escala Fahrenheit. Con el origen en -459,67 °F (aproximadamente)(desuso)
Conversión de temperaturas
Las siguientes fórmulas asocian con precisión las diferentes escalas de temperatura:
Temperatura en distintos medios
La temperatura en los gases
K = K | K = C + 273,15 | K = (F + 459,67) | K = Ra | K = Re + 273,15 | K = (Ro - 7,5) + 273,15 | K = N + 273,15 | K = 373,15 - De | |
C = K − 273,15 | C = C | C = (F - 32) | C = (Ra - 491,67) | C = Re | C = (Ro - 7,5) | C = N | C = 100 - De | |
F = K - 459,67 | F = C + 32 | F = F | F = Ra − 459,67 | F = Re + 32 | F = (Ro - 7,5) + 32 | F = N + 32 | F = 121 - De | |
Ra = K | Ra = (C + 273,15) | Ra = F + 459,67 | Ra = Ra | Ra = Re + 491,67 | Ra = (Ro - 7,5) + 491,67 | Ra = N + 491,67 | Ra = 171,67 - De | |
Re = (K − 273,15) | Re = C | Re = (F - 32) | Re = (Ra - 491,67) | Re = Re | Re = (Ro - 7,5) | Re = N | Re = 80 - De | |
Ro =(K - 273,15) +7,5 | Ro = C +7,5 | Ro = (F - 32) +7,5 | Ro = Ra - 491,67 +7,5 | Ro = Re +7,5 | Ro = Ro | Ro = N +7,5 | Ro = 60 - De | |
N = (K - 273,15) | N = C | N = (F - 32) | N = (Ra - 491,67) | N = Re | N = (Ro - 7,5) | N = N | N = 33 - De | |
De = (373,15 - K) | De = (100 - C) | De = (121 - F) | De = (671,67 - Ra) | De = (80 - Re) | De = (60 - Ro) | De = (33 - N) | De = De |
Para un gas ideal, la teoría cinética de gases utiliza mecánica estadística para relacionar la temperatura con el promedio de la energía total de los átomos en el sistema. Este promedio de la energía es independiente de la masa de las partículas, lo cual podría parecer contraintuitivo para muchos. El promedio de la energía está relacionado exclusivamente con la temperatura del sistema, sin embargo, cada partícula tiene su propia energía la cual puede o no corresponder con el promedio; la distribución de la energía, (y por lo tanto de las velocidades de las partículas) está dada por la distribución de Maxwell-Boltzmann. La energía de los gases ideales monoatómicos se relaciona con su temperatura por medio de la siguiente expresión:
, donde (n= número de moles, R= constante de los gases ideales).
El cálculo de la energía cinética de objetos más complicados como las moléculas, es más difícIl. Se involucran grados de libertad adicionales los cuales deben ser considerados. La segunda ley de la termodinámica establece sin embargo, que dos sistemas al interactuar el uno con el otro adquirirán la misma energía promedio por partícula, y por lo tanto la misma temperatura.
Sensación térmica
Es importante destacar que la sensación térmica es algo distinto de la temperatura tal como se define en termodinámica. La sensación térmica es el resultado de la forma en que la piel percibe la temperatura de los objetos y/o de su entorno, la cual no refleja fielmente la temperatura real de dichos objetos y/o entorno. La sensación térmica es un poco compleja de medir por distintos motivos:
- El cuerpo humano mide la temperatura a pesar de que su propia temperatura se mantiene aproximadamente constante (alrededor de 37 °C). Por lo tanto, no alcanza el equilibrio térmico con el ambiente o con los objetos que toca.
- Las variaciones de calor que se producen en el cuerpo humano generan una diferencia en la sensación térmica, desviándola del valor real de la temperatura. Como resultado, se producen sensaciones de temperatura exageradamente altas o bajas.
Temperatura seca
Se le llama temperatura seca del aire de un entorno (o más sencillamente: temperatura seca) a la temperatura del aire, prescindiendo de la radiación calorífica de los objetos que rodean ese ambiente concreto, y de los efectos de la humedad relativa y de los movimientos de aire. Se puede obtener con el termómetro de mercurio, respecto a cuyo bulbo, reflectante y de color blanco brillante, se puede suponer razonablemente que no absorbe radiación.
La temperatura radiante tiene en cuenta el calor emitido por radiación de los elementos del entorno.
Se toma con un termómetro de bulbo, que tiene el depósito de mercurio encerrado en una esfera o bulbo metálico de color negro, para asemejarlo lo más posible a un cuerpo negro y así absorber la máxima radiación. Para anular en lo posible el efecto de la temperatura del aire, el bulbo negro se aísla en otro bulbo que se fue hecho al vacío.
Las medidas se pueden tomar bajo el sol o bajo sombra. En el primer caso se tendrá en cuenta la radiación solar, y se dará una temperatura bastante más elevada.
También sirve para dar una idea de la sensación térmica.
La temperatura de bulbo negro hace una función parecida, dando la combinación de la temperatura radiante y la ambiental.
Temperatura de bulbo húmedo o temperatura húmeda, es la temperatura que da un termómetro bajo sombra, con el bulbo envuelto en una mecha de algodón húmedo bajo una corriente de aire. La corriente de aire se produce mediante un pequeño ventilador o poniendo el termómetro en un molinete y haciéndolo girar. Al evaporarse el agua, absorbe calor rebajando la temperatura, efecto que reflejará el termómetro. Cuanto menor sea la humedad relativa del ambiente, más rápidamente se evaporará el agua que empapa el paño. Este tipo de medición se utiliza para dar una idea de la sensación térmica, o en los psicrómetros para calcular la humedad relativa y la temperatura del punto de rocío.
Coeficiente de dilatación térmica
Artículo principal: Coeficiente de dilatación
Durante una transferencia de calor, la energía que está almacenada en los enlaces intermoleculares entre 2 átomos cambia. Cuando la energía almacenada aumenta, también lo hace la longitud de estos enlaces. Así, los sólidos normalmente* se expanden al calentarse y se contraen al enfriarse; este comportamiento de respuesta ante la temperatura se expresa mediante el coeficiente de dilatación térmica (unidades: °C-1):
- esto no ocurre para todos los sólidos: el ejemplo más típico que no lo cumple es el hielo.
Curiosidades
- La temperatura más alta registrada en nuestro planeta fue medida en el desierto de "El Azizia", en Libia. Allí, el 13 de septiembre de 1922, el termómetro marcó una temperatura de 57,8 ºC.
- La temperatura más baja jamás registrada fue en la Antártida, con -89,2 °C, cerca de la estación de Vostok, el 21 de julio de 1983, a 3420 m de altitud.
- El termómetro fue inventado en 1607 por Galileo.
- La temperatura media más alta fue registrada en Etiopía con 34,6 °C, entre los años 1960 y 1966.
- La temperatura media más baja fue registrada en la estación de Vostok, con -55,1 °C, entre los años 1961 y 1990.
- La temperatura más baja registrada en una zona habitada fue en Oymyakon, en Siberia, donde el 26 de enero de 1926, se registró una temperatura de -71,2 °C.
- La temperatura más alta alcanzada en el Polo Sur fue de -13,6 °C en 1978.
Referencias
BIOGRAFIA
- Wikimedia Commons alberga contenido multimedia sobre Temperatura.Commons
- Wikilibros alberga un libro o manual sobre Temperatura.
- Wikiversidad alberga proyectos de aprendizaje sobre Temperatura.Wikiversidad
- Wikcionario tiene definiciones para Temperatura.Wikcionario
- Conversor de Unidades de Temperatura
- Curiosidades
CONCLUSION : Ya hablando dela temperatura nos dice que todos los dias experimentamos ya sea con el calor o cuendo hace frio o cuando tenemos temperatura o cotidianamente al poner agua hervir o en el medio ambiente o todo lo que te rodea encotramos lo que es la temperatura y es una cantidad de energia que nosotros mismos transferimos a otro como consecuencia de temperatura entre ambos y eso nos permite clasificar los cuerpos en frio y calientes y da la idea de que la temperatura y por la extension de calor y durante un prolongado tiempo termina por alcanzar un estado de equilibrio entre ambos cuerpos que se denominan un equilibrio termico eso es lo que entendi sobre la temperatura.

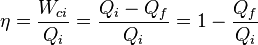 (1)
(1)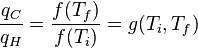 (2)
(2)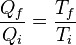 (3)
(3)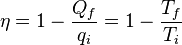 (4)
(4)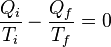 (5)
(5)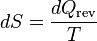 (6)
(6)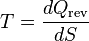 (7)
(7)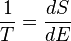 (8)
(8)

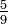
 + 273,15
+ 273,15 + 273,15
+ 273,15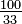 + 273,15
+ 273,15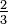
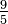 - 459,67
- 459,67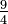 + 32
+ 32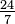 + 32
+ 32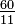 + 32
+ 32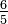
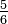
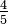
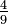
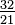
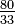
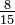
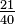 +7,5
+7,5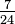 +7,5
+7,5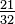 +7,5
+7,5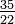 +7,5
+7,5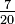
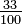
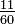
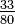
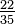
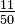
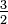
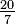
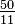
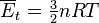 , donde (n= número de
, donde (n= número de 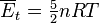
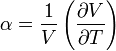
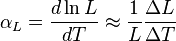
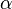 como la letra lambda
como la letra lambda 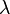 .
.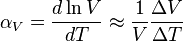
 La temperatura atmosférica es el indicador de la cantidad de energía calorífica acumulada en el aire. Aunque existen otras escalas para otros usos, la temperatura del aire se suele medir en grados centígrados (ºC) y, para ello, se usa un instrumento llamado "termómetro".
La temperatura atmosférica es el indicador de la cantidad de energía calorífica acumulada en el aire. Aunque existen otras escalas para otros usos, la temperatura del aire se suele medir en grados centígrados (ºC) y, para ello, se usa un instrumento llamado "termómetro".